Очистка воды |
 |
тел.: (495)755-64-37, |
 |
 |
 |
 |
 |
 |
||
| Обезжелезивание и деманганация водыВ. В. Банников, канд. техн. наук
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Характеристика фильтрующего слоя при обезжелезивании воды упрощенной аэрацией | Расчетная скорость фильтро- вания, м/ч | ||||
| Мин. диаметр зерен, мм | Макс. диаметр зерен, мм | Эквивалентный диаметр зерен, мм | Коэффициент неоднород- ности | Высота слоя, мм | |
| 0,8 | 1,8 | 0,9 -1,0 | 1,5 - 2 | 1000 | 5 - 7 |
| 1 | 2 | 1,2 - 1,3 | 1,5 - 2 | 1200 | 7 - 10 |
Используя характеристики конкретного наполнителя фильтра и руководствуясь параметрами табл. 1, можно выполнить расчет фильтровальной станции. СНиП [1] требует, чтобы продолжительность работы фильтров между промывками составляла при нормальном режиме не менее 8-12 часов и не менее 6 часов при форсированном режиме или при полной автоматизации промывки фильтра.
Общую поверхность фильтрования можно определить по формуле:
F = Q / (Tстvн - nпрqпр - nпрtпрvн), (1)
где Q - полезная производительность фильтровальной станции за 1 сутки, м3; Tст - продолжительность работы станции в течение суток, ч; vн - расчетная скорость фильтрования при нормальном режиме, м/ч, принимаемая по табл. 1, с учетом соотношения (3); nпр - число промывок одного фильтра в сутки при нормальном режиме эксплуатации; qпр - удельный расход воды на одну промывку одного фильтра, м3/м2 (определяется из паспортных данных фильтра и эксплуатационных характеристик наполнителя); tпр - время простоя фильтра в связи с промывкой, ч (определяется из паспортных данных фильтра и рабочих характеристик наполнителя).
Количество фильтров в составе фильтровальной станции производительностью более 1600 м3/сутки должно быть не менее четырех. При производительности более 8-10 тыс. м3/сутки количество фильтров N следует определять с округлением до ближайших целых чисел (четных или нечетных в зависимости от компоновки фильтров) по формуле:
N = (F)0,5 / 2 (2)
При этом должно быть выдержано соотношение:
Vф = Vн N / (N - N1) (3)
где N1 - число фильтров, находящихся в ремонте; Vф - скорость фильтрования при форсированном режиме.
Аэрация на специальных устройствах
Аэрация на специальных устройствах используется, когда необходимо удалить из воды железо при концентрации его в воде выше 10 мг/л и увеличить величину рН выше 6,8.
Для осуществления аэрации используют вентиляторные градирни (дегазаторы), либо контактные градирни с естественной вентиляцией. На рис. 1 представлена схема установки для обезжелезивания воды аэрацией. Исходная вода через патрубок 1подается в верхнюю часть вентиляторной градирни, заполненной керамической насадкой 4 (кольца Рашига размером 25х25х4 мм) или деревянной хордовой насадкой из брусков. Навстречу потоку воды с помощью вентилятора 5 направляют воздух. В процессе аэрации выделяется углекислота (диоксид углерода), а вода обогащается кислородом. Из градирни вода стекает в контактную емкость 7, откуда насосом подается в напорный фильтр. В объеме наполнителя фильтра завершается образование хлопьев гидроксида трехвалентного железа и их задержание.
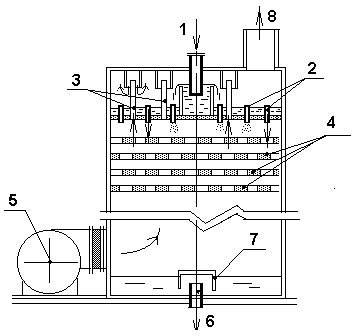
Рис. 1. Схема установки обезжелезивания воды аэрацией.
1 - патрубок для подачи исходной воды в вентиляторную градирню; 2 - водосливные трубки; 3 - воздушные трубки; 4 - насадка; 5 - вентилятор; 6 - патрубок для отвода обработанной воды; 7 - контактная емкость с гидравлическим затвором; 8 - патрубок для выхода газов из градирни.
Площадь поперечного сечения дегазатора вычисляется исходя из плотности орошения (Пор):
- керамическая насадка - 60 м3/ч на 1 м2 площади дегазатора,
- деревянная хордовая насадка - 40 м3/ч на 1 м2 площади.
Вентилятор дегазатора должен обеспечивать подачу не менее 15 м3 воздуха на каждый куб. метр обрабатываемой воды. Определение напора, развиваемого вентилятором, следует производить с учетом сопротивления насадки. На каждый метр высоты слоя керамической насадки «теряется» 30 мм вод. ст., а для деревянной хордовой - 10 мм вод. ст.
Время пребывания воды в контактной емкости tконт (после дегазатора) составляет 30-45 минут.
Высота слоя насадки, необходимая для снижения содержания диоксида углерода в воде, определяется с помощью табл. 2. Содержание диоксида углерода в воде, подаваемой в градирню (дегазатор) зависит от концентрации растворенного (равновесного) свободного диоксида углерода [СО2]св, мг/л и карбонатной жесткости исходной воды, разрушаемой при водоподготовке, мг-экв/л [1,4,2]:
[СО2] = ([СО2]св + 44 Жк) (4)
Таблица 2
| Содержание СО2 в воде, подаваемой на дегазатор, мг/л | Высота слоя насадки в дегазаторе, м | |
| Кислотоупорная керамическая | деревянная хордовая | |
| 1 | 2 | 3 |
| 50 | 3 | 4 |
| 100 | 4 | 5,2 |
| 150 | 4,7 | 6 |
| 200 | 5,1 | 6,5 |
| 250 | 5,5 | 6,8 |
| 300 | 5,7 | 7 |
Блок аэрационного окисления входит в состав установки «Деферрит», разработанной НИИ коммунального водоснабжения и очистки воды и выпускаемой предприятием «Водкоммунтех». Производительность установки по очищенной воде от 50 до 20000 м3/сут.
ПРИМЕР 1. Выполнить расчет установки обезжелезивания производительностью:
- суточная, Qсут - 12000 м3,
- часовая, Qчас - 500 м3.
Содержание двухвалентного железа в исходной воде равно 8 мг/л, величина рН = 7,1.
Концентрация свободного диоксида углерода - 35 мг/л, карбонатная жесткость - 4,5 мг-экв/л.
Для аэрации использовать дегазатор с вентилятором. Насадка дегазатора - кольца Рашига.
1. Требуемая площадь дегазатора Fдег, м2, определяем по формуле:
Fдег = Qчас / Пор
Плотность орошения дегазатора, заполненного кольцами Рашига, составляет 60 м3/ч.
Тогда: Fдег = 500/60 = 8,33 м2.
2. Диаметр дегазатора определим по формуле:
D = (4 Fдег/ 3,14)0,5 = (4*8,33 / 3,14)0,5 = 3,26 м.
3. С помощью выражения (4) определим содержание диоксида углерода в исходной воде: [СО2] = (35 + 44*4,5) = 233 мг/л.
Высота слоя насадки из колец Рашига Нр принимается в соответствии с таблицей 2 равной 5,5 м.
4. Производительность вентилятора дегазатора равна:
Qвент = 15 * Qчас = 15*500 = 7500 м3/ч.
5. Напор, который необходимо развивать вентилятору, равен:
Нвент = 30 * Нр = 30*5,5 = 165 м.
6. Объем контактной емкости:
Vконт = Qчас tконт /60 = 500*40/60 = 333,33 м3.
Если принять высоту слоя воды в контактной емкости в виде цилиндрического резервуара 8 м, то ее диаметр будет равен 7,3 м.
Коагуляция и осветление, известкование
Из поверхностных вод, как правило, необходимо удалить взвеси и коллоидно-дисперсные вещества, включающие соединения железа. Освобождение воды от взвеси и коллоидных веществ возможно осуществить только путем ввода специальных реагентов-коагулянтов. Данный метод обработки воды называют коагуляцией. Коагулянт образует в воде хлопья, которые адсорбируют на своей поверхности коллоиды и выделяются в виде осадка.
Рабочий режим и оборудование для осветления и коагуляции исходной воды выбирают исходя из характера и уровня содержания загрязнений. При этом если необходимо одновременно повысить щелочность воды и снизить ее солесодержание, рассматриваемые процессы совмещают с известкованием.
Процесс коагуляции достаточно сложен и нет строгих стехиометрических соотношений между дозой коагулянта и количеством растворенных коллоидных веществ в исходной воде. Поэтому дозу определяют методом пробного коагулирования.
В качестве коагулянтов применяют:
- сульфат алюминия (глинозем) Al2(SO4)3 * 18 H2O при рН исходной воды 6,5-7,5;
- сульфат железа (железный купорос) FeSO4 * 7 H2O при рН воды 4-10;
- хлорное железо FeCl3 * 6 H2O для воды с рН 4-10.
Для интенсификации процесса коагуляции в воду дополнительно вводят флокулянты (наиболее распространен полиакриламид). Флокулянты способствуют укрупнению осадка и ускоряют процесс слипания осаждаемых коллоидных и взвешенных частиц [7].
При достаточном содержании в воде карбонатной жесткости (выше 1 мг-экв/л) коагулянты вначале образуют неустойчивые бикарбонаты (реакции 4), которые разлагаются с образованием хлопьев гидроксидов (реакции 5):
Al2(SO4)3 + 3 Са(HCO3)2 = 2 Al(HCO3)3 + 3 CaSO4 (4)
FeSO4 + Ca(HCO3)2 = Fe(HCO3)2 + CaSO4
2 Al(HCO3)3 = 2 Al (OH)3↓ + 6 CO2 (5)
4 Fe(HCO3)2 + O2 + 2 H2O = 4 Fe(OH)3↓ + 8 CO2
По реакции 5 видно, что для образования хлопьев гидроксида железа необходимо наличие в воде растворенного кислорода.
Если карбонатная жесткость исходной воды невелика, то ее подщелачивают раствором гидроксида натрия или «известковым молоком» (раствор Ca(OH)2):
4 FeSO4 + 4 Ca(OH)2 + 2 H2O + O2 = 4 Fe(OH)3 ↓ + 4 CaSO4 (6)
Осветление и обесцвечивание мутных вод с повышенной жесткостью предпочтительнее осуществлять коагулянтами при высоких значениях рН, а цветных мягких вод - при пониженных рН.
При реализации процесса коагуляции температуру воды поддерживают в пределах 20-25 оС, а при осуществлении коагуляции с известкованием воду подогревают до 30-40 оС.
Дозу коагулянта сульфата алюминия обычно принимают в пределах 0,5-1,2 мг-экв/л. Для воды с умеренным (до 100 мг/л) содержанием взвеси и с небольшой окисляемостью дозу понижают, а для вод с содержанием железа и с высокой окисляемостью (15 мг/л О2 и выше) ее повышают до 1,5 мг-экв/л. Для цветных вод дозу можно ориентировочно определить по формуле [7]:
Дк = 4 (Ц)0,5, (5)
где Дк - доза коагулянта, мг/л; Ц - цветность воды, градусы.
Дозировка флокулянта полиакриламида в виде 0,1 %-ого раствора составляет 0,1-1,0 мг на каждый литр обрабатываемой воды (в пересчете на 100%-ный продукт). Флокулянт добавляют спустя 1-3 минуты после дозирования коагулянта с целью завершения формирования микрохлопьев и адсорбции загрязнений.
При необходимости подщелачивания воды дозу щелочи можно определить из выражения:
Дщ = Эщ(Дк/Эк - Щ + 1)*100/С, (6)
где Дщ - доза щелочи, мг/л;
Эщ - эквивалентная масса активной части пощелачивающего реагента, равная для извести 28 (в пересчете на СаО) и 53 для соды (в пересчете на Na2CO3), мг/мг-экв;
Эк - эквивалент безводного коагулянта, равный 57,02 мг/мг-экв для Al2(SO4)3; 75,16 - FeSO4; 54,07 - FeCl3;
Щ - общая щелочность исходной воды + 1 (резервная щелочность), мг-экв/л;
С - концентрация активного вещества в реагенте для подщелачивания, %.
Если величина Дщ при расчете по выражению (6) отрицательна, то подщелачивания не требуется.
Когда в исходной воде содержание взвешенных веществ менее 100 мг/л, коагуляцию осуществляют непосредственно на осветлительных фильтрах с дозировкой коагулянта в подающий трубопровод. Расстояние от точки ввода коагулянта до фильтра должно составлять ≥ 50 диаметров трубопровода (50 Dу).
При концентрации взвеси более 100 мг/л в обрабатываемую воду помимо коагулянта вводят полиакриламид с соответствующим временным разрывом, а процесс ведут в осветлителе.
Дозирующие насосы подбирают исходя из максимальной дозы коагулянта. Cуточный расход коагулянта (в пересчете на безводный 100 %-ный продукт, кг) определяют по формуле:
Pк = 24*Qчас*Эк*Дк/1000, (7)
где Qчас - производительность установки по воде, м3/ч;
Эк - эквивалент безводного коагулянта, равный 57,02 для Al2(SO4)3; 75,16 - FeSO4; 54,07 - FeCl3;
Дк - максимально требуемая доза коагулянта, мг-экв/л.
Расход раствора коагулянта находят при помощи следующего соотношения:
Vк = 100 *Рк / (Ск*ρк), (8)
где Vк - суточный объем раствора коагулянта, м3/сутки;
Ск - концентрация коагулянта в дозируемом растворе, обычно равна 5-10 %;
ρк - плотность раствора коагулянта, кг/м3.
Введение реагентов-окислителей
Использование реагентов-окислителей, в первую очередь хлора, с целью обеззараживания, а также удаления железа, используется в России с начала ХХ века. Кульский Л.А. [8] указывал, что хлорирование почти во всех случаях освобождает воду от содержащегося в ней железа. После обработки разных вод этим методом содержание железа во всех случаях остается меньше 0,1 мг/л, причем этот метод эффективен, когда другие приемы не работают. Под действием хлора происходит разрушение гуматов и других органических соединений железа и переход их в форму неорганических солей трехвалентного железа, которые легко гидролизуются. В результате гидролиза выпадает осадок гидроксида железа, либо продуктов неполного гидролиза - основных солей железа различного состава. Эти процессы можно условно описать следующим брутто-уравнением:
4 Fe(HCO3)2 + 2 Cl2 + 4 H2O = 4 Fe(OH)3↓ + 8 CO2↑ + 4 HCl (7)
Как видно из уравнения (7) вода подкисляется. По стехиометрии (по уравнению реакции) на окисление 1 мг двухвалентного железа расходуется 0,64 мг хлора, при этом щелочность снижается на 0,018 мг-экв/л.
Хлор также окисляет двухвалентный марганец, разрушает органические вещества и сероводород.
Доза хлора в зависимости от содержания железа может составлять 5-20 г на 1 куб. метр воды при контакте, по крайней мере, 30 минут (не только для окисления железа, но и для надежного обеззараживания). При этом гигиенические требования допускают содержание свободного хлора в питьевой воде до 0,5 мг/л, а связанного до 1,2 мг/л.
СНиП [1] определяет расчетную дозу хлора (в пересчете на 100 %, мг/л) для целей обезжелезивания следующим выражением:
Дх = 0,7 * [Fe2+], (9)
где [Fe2+] - концентрация двухвалентного железа в мг/л.
Дозу активного хлора для целей обеззараживания воды устанавливают на основе данных технологических изысканий. Если они отсутствуют, то для предварительных расчетов следует принимать 2-3 мг/л для поверхностной фильтрованной воды, 0,7-1,0 мг/л для вод из подземных источников.
Обработку воды хлором осуществляют с помощью хлораторов, в которых газообразный (испаренный) хлор абсорбируют водой. Хлорную воду из хлоратора подают к месту потребления. Хотя данный метод обработки воды и является наиболее распространенным, тем не менее, он обладает целым рядом недостатков. В первую очередь это связано со сложной транспортировкой и хранением больших объемов жидкого высокотоксичного хлора. На станциях водоподготовки необходимо наличие экологически опасных стадий хлорного хозяйства, таких как разгрузка емкостей с жидким хлором, его испарения для перевода в рабочую форму. Создание рабочих запасов хлора на складах представляет опасность не только для рабочего персонала станции, но и для населения [9].
Как альтернативу хлорированию в последние годы все шире используют обработку воды раствором гипохлоритом натрия (NaClO), причем этот метод находит применение, как на больших станциях водоподготовки, так и на небольших объектах, в том числе и в частных домах.
Водные растворы гипохлорита натрия получают химическим:
Cl2 + 2 NaOH = NaClO + NaCl + H2O, (8)
или электрохимическим методом:
NaCl + H2O = NaClO + H2, (9).
В соответствии с [10] раствор гипохлорита натрия, получаемый по химическому методу, выпускается в виде трех марок. Ниже приведены показатели по составу продуктов.
| Марка | «А» | «Б» | «В» |
| Содержание: | |||
| активный хлор, г/л | 190 | 170 | 120 |
| гидроксид натрия, г/л | 10-20 | 40-60 | 20-90 |
Обеззараживание воды и окисление примесей с использованием гипохлорита натрия, производимого электрохимически, впервые было применено в США в конце 30-х годов прошлого столетия. Дальнейшее развитие электрохимии, разработка конструкций новой электрохимической аппаратуры с использованием современных стойких электродных материалов, позволило создать установки, способные конкурировать с другими методами обеззараживания воды [9, 13].
В качестве примера можно указать электрохимические установки серии «Санатор®», разработанные и выпускаемые предприятием «Экосервис Технохим». Установка «Санатор®» готовит гипохлорит натрия из поваренной соли непосредственно на месте потребления. Кроме того, они снабжены устройством пропорционального дозирования раствора гипохлорита в подающий трубопровод перед фильтрами. На рис. 2 показана схема подачи гипохлорита в магистральный трубопровод, на рис. 3 принципиальная схема подключения установки.
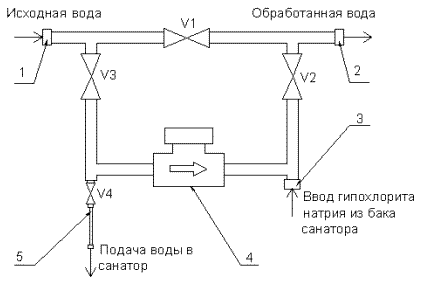
Рис. 2. Схема подключения трубной сборки.
1 - патрубок подачи исходной воды; 2 - патрубок вывода обработанной воды; 3 - патрубок с обратным клапаном для подачи раствора гипохлорита натрия; 4 - водосчетчик; 5 - гибкий шланг с накидной гайкой; V1-V4 - шаровые краны.
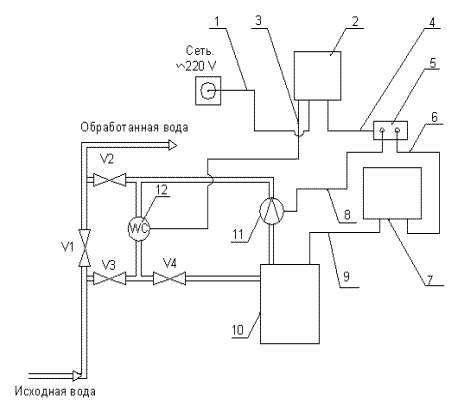
Рис.3. Принципиальная схема подключения Санатора.
1 - сетевой кабель; 2 - микроконтроллер; 3 - кабель импульсного вывода; 4 - кабель нагрузки; 5 - распределительная колодка (розетки); 6 - кабель подключения блока питания; 7 - блок питания Санатора; 8 - кабель подключения дозирующего насоса; 9 - кабель подключения электродной кассеты; 10 - бак Санатора; 11 - дозирующий насос; 12 - водосчетчик; V1-V4 - шаровые краны.
Гипохлорит натрия обладает рядом свойств, ценных в техническом отношении. Его водные растворы не имеют взвесей и поэтому не нуждаются в отстаивании, например, в противоположность хлорной извести. Применение гипохлорита натрия для обработки воды не вызывает увеличения ее жесткости, так как он не содержит солей кальция и магния как хлорная известь или гипохлорит кальция. Бактерицидный эффект раствора NaClO, полученного электролизом, выше, чем у других дезинфектантов, действующим началом которых является активный хлор. Кроме того, он обладает еще большим окислительным действием, чем растворы, приготовленные химическим методом из-за более высокого содержания хлорноватистой кислоты (HClO).
Окисление двухвалентного железа происходит в соответствии со следующим уравнением:
2 Fe(HCO3)2 + NaClO + H2O = 2 Fe(OH)3↓ + 4 CO2↑ + NaCl (10)
Расчет установки для обработки воды гипохлоритом натрия в первую очередь требует определить расход активного хлора на процессы окисления, обеззараживания и разрушение сероводорода.
Требуемый расход активного хлора на обработку воду АХ (в пересчете на 100% хлор, г/ч) определяется следующим выражением:
AX = Qчас * {Дх + [Fe2+] * KFe] + [Mn2+] * KMn + [H2S] * KCB}, (9)
где Qчас - объемный расход воды (максимальный), м3/ч;
Дх - доза активного хлора для обеззараживания воды, мг/л;
[Fe2+] - содержание двухвалентного железа в исходной воде, мг/л;
KFe - расход активного хлора для окисления железа (0,67 мг активного хлора на 1 мг двухвалентного железа);
[Mn2+]- содержание двухвалентного марганца в исходной воде, мг/л;
KMn - расход активного хлора для окисления двухвалентного марганца (1,3 мг активного хлора на 1мг марганца);
[H2S] - содержание сероводорода в исходной воде, мг/л;
KCB - расход активного хлора для разрушения сероводорода (2,1 мг активного хлора на 1 мг сероводорода).
Как следует из уравнения реакции (10) в процессе окисления железа гипохлоритом натрия не происходит подкисления воды, а это очень важно для процесса фильтрации. Кроме того, раствор гипохлорита натрия как товарный, так и электрохимический, щелочной, что благоприятно для фильтрования.
ПРИМЕР 2. Выполнить расчет установки для обработки воды товарным раствором гипохлорита натрия марки «Б»[10] с содержанием активного хлора 170 г/л. Раствор перед введением гипохлорита разбавить в 17 раз (Кр-коэффициент разбавления) до концентрации Ср=10 г/л (рабочий раствор).
Часовая производительность установки по воде, Qчас - 5,5 м3,
суточный расход воды, Qсут - 88 м3, т.е. установка работает t=16 часов в сутки.
Состав исходной воды:
- двухвалентное железо 8 мг/л,
- двухвалентный марганец 0,5 мг/л,
- сероводород 0,4 мг/л,
- величина рН = 6,9.
Пробная обработка воды показала необходимость введения 3,5 мг/л активного хлора для целей обеззараживания.
1. Требуемый расход активного хлора (в пересчете на 100%) определим по выражению (9):
АХ = 5,5 * (3,5 + 8*0,67 + 0,5*1,3 + 0,4*2,1) = 56,9 г/ч.
2. Скорость подачи рабочего раствора гипохлорита натрия (необходима для подбора дозирующего насоса по производительности):
Пгн = АХ / Ср = 56,9 / 10 ≈ 6 л/ч.
3. Суточный расход рабочего раствора гипохлорита (необходим для подбора бака для хранения и дозирования рабочего раствора):
Пгн * t = 6*16 = 96 л.
4. Суточный расход товарного раствора гипохлорита натрия марки «Б» (необходим для определения затрат на реагент):
Ргн = Пгн * t / Кр = 6 * 16 / 17 = 5,6 л.
Используется также метод окисления двухвалентного железа путем введения в исходную воду перед фильтрами раствора перманганата калия KMnO4. Последний может также вводиться в сочетании с гипохлоритом натрия с целью обработки сложных вод и экономии достаточно дорогостоящего окислителя - перманганата калия.
При обработке воды перманганатом реакция окисления железа с последующим гидролизом протекает по уравнению (упрощенная запись):
4 Fe(HCO3)2 + MnO4 - + 2 H2O = 4 Fe(OH)3↓ + MnO2↓ + 8 CO2↑ (11)
По уравнению (11) на окисление 1 мг Fe2+ тратится 0,71 мг перманганата калия, а щелочность воды снижается на 0,036 мг-экв/л. СНиП [1] определяет расчетную дозу перманганата калия (в пересчете на 100 %, мг/л) для окисления железа и марганца при помощи следующего выражения:
Дпк = [Fe2+] + 2* [Mn2+], (10)
где [Fe2+] - концентрация двухвалентного железа в исходной воде, мг/л;
[Mn2+] - концентрация двухвалентного марганца, мг/л.
Для приготовления рабочих растворов перманганата калия следует руководствоваться данными по растворимости перманганата в воде:
- при температуре 20 0С 6,34 г KMnO4 на100 г воды;
- при 60 0С 22,2 г KMnO4 на100 г воды.
При совместном введении в обрабатываемую воду перманганата калия и гипохлорита натрия дозы этих реагентов (в пересчете на 100% продукт, мг/л) можно определить из уравнений:
Дпк = 0,2*[Fe2+] + 2* [Mn2+], (11)
Дгн = 0,7*[Fe2+].
При сравнении уравнений (10) и (11) следует, что совместный ввод реагентов позволяет сэкономить до 80% перманганата калия. Введение перманганата перед подачей гипохлорита натрия разрушает органические вещества, вступающие в реакцию с хлором с образованием продуктов с резким запахом, например фенолы. Если ввод реагентов осуществить в другой последовательности, то перманганат калия будет разрушать образованные хлорпродукты.
Одним из перспективных методов окисления железа является озонирование. Озон О3 является одним из самых сильных окислителей, уничтожающих бактерии, споры и вирусы. По сравнению с хлором применение озона оказывается более эффективным для окисления детергентов, гербицидов, пестицидов, фенолов и для окисления других трудно окисляемых химических соединений. Одновременно с обеззараживанием идут процессы окисления двухвалентных железа и марганца, обесцвечивание воды, а также ее дезодорация и улучшение органолептических свойств.
Озон получают из воздуха в специальных аппаратах - озонаторах. В озонаторе при прохождении электрического тока через разрядное пространство с воздухом происходит разряд коронного типа, в результате чего из кислорода воздуха образуется озон.
По стехиометрии можно определить дозу озона на окисление двухвалентного железа по следующему выражению:
Доз = 0,14 * [Fe2+], мг/л (12)
где [Fe2+] - концентрация двухвалентного железа в исходной воде, мг/л.
Доза озона зависит от цели, для которой используют озонирование воды. Для обеззараживания фильтрованной воды доза озона составляет 1-3 мг/л, для обработки подземных вод - 0,75-1 мг/л. При введении озона для окисления железа, обесцвечивания воды с одновременным обеззараживанием доза может доходить до 4 мг/л. Озоно-воздушную смесь из озонатора вводят в воду с помощью эжекторов или через сеть пористых труб, уложенных в камерах смешения.
Концентрация остаточного озона после камер смешения должна быть 0,1-0,3 мг/л. Продолжительность контакта озона с водой зависит от состава воды, концентрации озона в озоно-воздушной смеси, конструкции смесителя, температуры и в среднем составляет 5-20 минут, часто 5-12 минут.
Наша промышленность производит низкочастотные озонаторы, работающая на токе промышленной частоты, а также высокочастотные (0,4-10 кГц), которые более компактные и менее металлоемкие. Завод «Курганхиммаш» серийно выпускает озонаторы производительностью по озону от 0,25 до 10 кг/ч.
Необходимо отметить, что озон высокотоксичен и может поражать органы дыхания. Предельно-допустимая концентрация озона в воздухе рабочей зоны (ПДК р.з.) составляет 0,1 мг/м3. Для сравнения можно указать, что для хлора эта величина в 10 раз менее жесткая и равна 1 мг/м3.
Хотя метод озонирования имеет блестящие перспективы, однако оборудование пока достаточно дорогостоящее, а процесс характеризуется сравнительно большим расходом электроэнергии.
Удаление воды из железа методом ионного обмена (катионирование) допускается, когда одновременно с обезжелезиванием требуется умягчение воды. Однако в этом случае, возможно, только извлечь железо в растворенной двухвалентной форме, а ресурс работы ионообменного материала будет значительно снижен. При этом в очищаемой воде должен отсутствовать кислород.
| Предыдущая страница | Следующая страница |
 |
ДЛЯ РЕШЕНИЯ ПРОБЛЕМ |
Собственное производство: |
|
|
Производство «GE Water & Process Technologies», «Wave Cyber», «Stenner», «AquaPro»: |
|
|
|
|



